Plasticità Sinaptica
Quando si parla di
“plasticità” ci si riferisce, di solito, alla particolare proprietà che ha un
solido di subire deformazioni di notevole ampiezza che permangono al cessare
della sollecitazione che le ha prodotte.
L’impiego
scientifico di questo termine ha trovato ovvia collocazione in discipline come
la fisica e l’ingegneria con lo scopo di descrivere le proprietà meccaniche
tipiche di alcuni materiali. Solo in tempi più recenti il termine “plasticità”
ha trovato applicazione anche in campo neurobiologico, con riferimento alla
“modificabilità” dimostrata dal sistema nervoso in risposta all’esposizione di
determinate “esperienze”. I fenomeni plastici all’interno del sistema nervoso
centrale (SNC) rappresentano ormai la necessaria premessa teorica per poter
ipotizzare interventi finalizzati a contenere o a superare esiti di patologie
anche molto gravi che costituiscono il presupposto fondamentale per la
formulazione di qualsiasi intervento riabilitativo. Parallelamente, si è andato
sempre più affermando in campo scientifico il concetto che vede la sfera
cognitiva collegata a quella motoria.
Studi effettuati
sugli animali e sull’uomo hanno confermato che l’esercizio agisce positivamente
su diversi aspetti del funzionamento cerebrale, sull’apprendimento e sulla
memoria, proteggendo dalla neurodegenerazione e alleviando la depressione.
Il movimento
aumenta la plasticità sinaptica, modificando direttamente la struttura della
sinapsi e potenziandone la forza, rafforzando allo stesso tempo i sistemi che
supportano la plasticità, come il metabolismo e la funzione vascolare.
Queste
modificazioni strutturali e funzionali sono state dimostrate in diverse aree
cerebrali, ma gli studi più significativi sono stati condotti a livello
ippocampale.
LTP ''Long Term Potentation''
La plasticità sinaptica è la capacità del sistema
nervoso di modificarsi al fine di apprendere, memorizzare nuove informazioni e
reagire a eventuali lesioni. I meccanismi responsabili di questi continui
cambiamenti vengono ricondotti alla forza delle sinapsi esistenti. Quest’ultime
possono essere modificate per periodi che vanno da alcuni millisecondi a
diversi mesi. Il glutammato è alla base di cambiamenti di lunga durata della
forza sinaptica che possono esser causati da brevi periodi di attività neuronale,
e principalmente da due processi detti potenziamento a lungo termine (LTP),
che aumenta la forza sinaptica, e depressione a lungo termine (LTD), che
la diminuisce. LTP e LTD sono termini
generali che vanno a descrivere la direzione della modificazione dell’efficacia
sinaptica. Tali forme di plasticità e vengono mediate da differenti meccanismi
di trasduzione del segnale nelle cellule nervose coinvolte.
Il glutammato viene rilasciato come trasmettitore
in molte sinapsi eccitatorie del sistema nervoso centrale. Esistono diversi
tipi di recettori per il glutammato. In Particolare, per quanto riguarda i
fenomeni di plasticità sinaptica, svolgono funzioni fondamentali i recettori
ionotropici NMDA (agonista del glutammato) e AMPA [1]-[2]. Nella maggior parte delle sinapsi, i recettori
AMPA formano canali permeabili al Na+ ed impermeabili al Ca2+. I recettori NMDA
sono invece permeabili al Ca2+, ma la loro attività è inibita dagli ioni Mg2+,
che vengono intrappolati all'interno del canale ionico. Durante la trasmissione
sinaptica di base vengono attivati i recettori AMPA, mentre quelli NMDA
risultano bloccati.
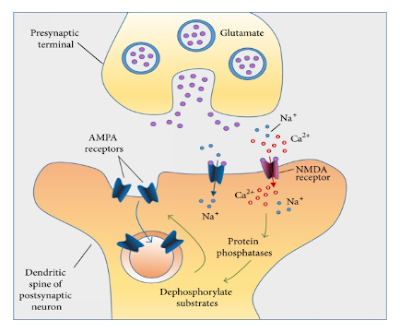
L'attivazione dei recettori NMDA è resa possibile
dalla depolarizzazione di membrana della spina dendridica determinata da una
stimolazione tetanica, che rimuove gli ioni Mg2+ dal canale ionico, permettendo
l’entrata degli ioni Ca2+ attraverso il canale NMDA (Fig.1). .
Figura 1
Fonte: https://www.researchgate.net/figure/LTD-mechanism-a-Ca2-ions-enter-in-small-quantities-through-NMDA-receptors-b_fig2_284032093
L’ingresso del calcio all’interno delle spine
dendritiche del neurone post sinaptico produce un aumento dell’ampiezza dei
potenziali post sinaptici, dunque il potenziamento a lungo termine (LTP)[2].
Nello specifico, l’entrata del calcio determina una serie di eventi
intracellulari, legati all’attivazione delle protein chinasi (per esempio la
protein chinasi A, PKA). Tali proteine, una volta attivate, determinano la
fosforilazione del fattore chiave per la trascrizione genica, CREB.
Quest’ultimo promuove la trascrizione di numerosi geni specifici, per la
trascrizione di nuove proteine e dei geni che codificano il fattore neutrofico
BDNF (Brain-Derived-Neutrofic-Factor), che favorisce la sopravvivenza dei
neuroni.
Il potenziamento a lungo termine è stato
riscontrato in molte vie sinaptiche. L’LTP può richiedere modalità di
stimolazione diverse in casi diversi, può decadere con diverso andamento e può
implicare meccanismi differenti [3-4].
Il ruolo dei recettori NMDA dell’ippocampo, è
quello di indurre l’LTP. Esistono a sua volta, dei recettori agonisti del NMDA
che bloccano l’induzione dello stesso. L’LTP non si riduce, se i recettori
intervengono, nel momento in cui il processo è stato indotto. [7-8].
Le ricerche sull’LTP cominciarono intorno al 1970
in Inghilterra, quando Timothy Bliss e i suoi colleghi scoprirono che una
stimolazione elettrica ad alta frequenza di pochi secondi poteva aumentare la
trasmissione sinaptica dell’ippocampo di coniglio per giorni o anche per
settimane [5].
Molto del lavoro sperimentale sull’LTP si è
concentrato sulle connessioni tra le collaterali di Schaffer e i neuroni
piramidali della regione CA1. Se si vanno a stimolare elettricamente le
collaterali di Schaffer si dà origine a potenziali post sinaptici eccitatori
(EPSP) nei neuroni postsinaptici della regione CA1. Se le collaterali di
Schaffer ricevono una stimolazione due o tre volte al minuto, l’ampiezza
dell’EPSP rimane costante. Se viene mandata una stimolazione tetanica, ovvero
un breve treno di impulsi ad alta frequenza sulle stesse collaterali, si ha la
generazione dell’LTP: un prolungato aumento dell’ampiezza dell’EPSP.
L’LTP possiede diverse proprietà [6]:
v È un fenomeno stato-dipendente. Come si è detto precedentemente, la possibilità che l’LTP avvenga è
determinato dal grado di depolarizzazione della cellula post sinaptica. Se si
stimolano le collaterali con un singolo stimolo in concomitanza con una forte
depolarizzazione delle cellule postsinaptiche CA1, aumenta l’ampiezza
dell’EPSP. Ciò si verifica solo in un intervallo di 100 millisecondi, dopo la
liberazione del neurotrasmettitore presinaptico;
v Gode di specificità. Quando l’LTP viene indotta dalla stimolazione
di una data sinapsi, essa non si verifica in altre sinapsi inattive che si
trovano sullo stesso neurone. L’LTP dipende specificatamente dalla terminazione
afferente. Questa caratteristica è concomitante con il processo di
memorizzazione e di apprendimento: se l’attivazione di un gruppo di sinapsi portasse
al potenziamento di tutte le altre sinapsi, comprese quelle inattive,
risulterebbe difficile il processo di selezionamento di determinate afferenze;
v Gode dell’associatività. Come è stato già affrontato, una debole
stimolazione non è sufficiente a innescare il potenziamento a lungo termine. Se
si attiva una debole stimolazione e contemporaneamente si da luogo anche ad una
forte stimolazione ad una via adiacente, si genera l’LTP nelle sinapsi
appartenenti ad entrambe le vie. L’associatività è la caratteristica che ha il
compito di collegare tra loro le diverse informazioni.
Referenze
1)
Casi clinici del substrato anatomico della memoria
dichiarative (H.M, N.A, R.B) Neuroscience, 31, 601-603
2)
Madison, D.V.,
Malenka, R.A. e Nicoll, R.A. Annu. Rev.
Neuros, 14, pp 379-397, 1991
3)
Brown, T.H., Kairiss, E.W. e Keenan, C.L., Annu. Rev. Neuroscience, 13, pp 475-551, 1990
4)
Collingridge,
G.L., Kehl, S.J e McLennan, H., J.
Physiol., 334, pp 33-46, 1983
5)
La nfield, P.W., S.A. 1988, Long-term potentation: From Biophysics to Behaviour. New York, A.R. Liss
6)
Papez, J.W. (1937) A proposed mechanism of emotion. Arch. Neurol, Psychiat 38: 725-743
7)
Muller, D., Joly, M. e Lynch, G., Science, 242, pp 1694-1697, 1988
8)
Bliss, T.V.P (1973) Long-Lasting potentation of synaptic transmission in the dentate area
of the anaesthetizeld rabbit following stimulation of perforant path, J.
Physiol, 232: 331-356









Nessun commento:
Posta un commento